关键词:昆虫细胞表达系统,杆状病毒表达载体系统,蛋白质表达,真核表达系统
1 蛋白表达系统概述
原核表达系统主要有大肠杆菌表达系统和枯草芽孢杆菌表达系统。1983年有两个课题组在大肠杆菌中表达了真核生物的基因 (Harris et al. 1983;Wetzel and Goeddel 1983)。因大肠杆菌在其遗传、生物化学与分子生物学方面已经被了解得比较透彻,所以它是许多外源蛋白表达的首选系统。大肠杆菌表达系统最大的特点是培养费用低、耐受能力强,并且能够高效地表达外源蛋白,其缺点是不能进行表达后修饰。枯草芽孢杆菌表达系统的优点是目的蛋白能以可溶的活性形式高产量地分泌到培养基中,但在蛋白表达过程中枯草芽孢杆菌会分泌一些蛋白酶降解目的蛋白,并且这个系统的表达量往往低于大肠杆菌表达系统。
目前常用的真核表达系统中有:哺乳动物细胞表达系统、酵母表达系统和杆状病毒表达系统(也称为昆虫细胞表达系统)。哺乳动物表达系统有许多优点:(1)表达的蛋白能进行翻译后修饰并正确的折叠;(2)能组成性或诱导性地表达目的蛋白;(3)目的蛋白还能以转基因形式表达(Colosimo et al. 2000)。但是,哺乳动物表达系统表达速度较慢,花费较高,并不适合用于蛋白大规模生产。酵母表达系统主要使用的是酿酒酵母和毕赤酵母。酵母表达系统的优势主要有两个方面,一方面是酵母中能进行蛋白表达后修饰,且它比哺乳动物表达系统成本低。另一方面是它表达的目的蛋白先在酵母细胞内,然后通过酵母的分泌系统,分泌到培养基中,得到折叠及修饰后的蛋白(Byrne et al. 2005)。但是,酵母细胞中蛋白的糖基化与哺乳动物中天然蛋白质的糖基化不同。因此,当目的蛋白的糖基化是保持蛋白活性的关键时,不应该选择酵母表达系统(Higgins et al. 1998)。酵母表达系统另一个缺点是大多的重组蛋白在这个系统中表达效率较低。相对于另外几个系统,杆状病毒/昆虫细胞(BEVS, Baculovirus expression vector system)是一个比较折中的蛋白表达体系(下图):

几种表达系统的对比
杆状病毒作为外源基因表达载体的优势主要有以下几个方面:
(1)易于操作。杆状病毒基因组较小,分子生物学特性比较简单,并且基因组上有多种限制性内切酶酶切位点。
(2)容纳的外源基因大。杆状病毒的病毒粒子是杆状的,容纳外源基因可塑性比较强,理论上它能容纳任何外源基因。
(3)能高效表达外源基因。在杆状病毒基因中p10基因和多角体蛋白基因都是极晚期基因,它们的启动子能够高效表达目的蛋白。
(4)能对目的蛋白进行表达后修饰。杆状病毒的宿主为昆虫细胞,目的蛋白可以利用昆虫细胞的翻译后修饰系统进行加工和修饰。
(5)安全性高。杆状病毒表达载体特异性非常强,只能够在昆虫细胞中进行复制。
(6)成本低。与哺乳动物细胞比较,昆虫培养细胞系相对更易于生长,并且昆虫细胞能悬浮培养可大量生产目的蛋白。
但是,杆状病毒表达载体也存在一些缺点。杆状病毒-昆虫细胞表达系统是一个瞬时表达系统。并且杆状病毒表达载体的启动子为晚期启动子表达时限是从感染后22-24小时开始至宿主细胞死亡,蛋白高水平表达时间很短。昆虫细胞一般不提供复杂的N-糖基化。虽然这种类型的N-糖基化通常足以提供有生物活性的蛋白产物,但是末端缺乏复杂糖基化有可能影响蛋白的溶解性和稳定性。另外,杆状病毒高水平表达蛋白的同时会致使细胞翻译后修饰的速度跟不上表达的速度,可能会降低产生表达后修饰蛋白。目前,杆状病毒-昆虫细胞表达系统已经广泛应用于人类健康、医学、农业等领域。
2 杆状病毒表达载体的研究进展
AcMNPV遗传图谱初步确定后,科学家们开始探索AcMNPV基因组的功能。1980 Summers等把多角体基因定位到了AcMNPV图谱上,之后Vlak等(1981)准确地定义了多角体基因的位置。随后,Rohrmann课题组(1982)确定了多角体基因的转录方向及编码氨基末端的区域。同年,Smith和Esche报道了AcMNPV基因组转录图谱。Smith把6个早期和13个晚期多肽确认并映射到了AcMNPV基因组上,并且把多角体蛋白基因更准确的定位到图谱上。1983年,Roche和Smith把极晚期基因p10定位到图谱上。在这些基础上,Smith等人定向突变多角体蛋白基因并且在多角体基因启动子下插入了外源基因,这同时也证明了多角体蛋白是非必须基因。
1983年,Smith首次在AcMNPV多角体启动子下成功克隆并表达了人的β-干扰素。同一时间,Hooft等报道了多角体基因的核苷酸序列。并且Pennock印证了产生重组病毒的方法,并通过分选出的重组病毒表达多角体蛋白-β-半乳糖苷酶的融合蛋白。随后,杆状病毒表达载体系统(baculovirus expression vector system,BEVS)开始在昆虫中表达目的蛋白。随着对杆状病毒上启动子的研究越来越透彻,发现杆状病毒启动子能够单独或与多角体蛋白启动子联合表达单个或多个外源蛋白。这个发现也为后来杆状病毒表达载体的发展提供了很重要的基础。在这个过程中研究者们定位了AcMNPV高效表达基因p10并测得其序列,之后构建了用p10启动子表达外源蛋白的AcMNPV。1988年Vlak等证明p10是非必须基因,并且在p10的位点上用p10启动子表达了β-半乳糖苷酶的融合蛋白。
1987年Emery和Bishop把多角体的启动子克隆到质粒上,然后与敲除多角体基因的AcNPV DNA共转染到草地贪夜蛾昆虫细胞中,在细胞内重组产生重组病毒,这个发现对BEVS的发展有重大的意义。首先,在AcMNPV基因上鉴定了几个非必需位点(p10、多角体蛋白基因位点),这些位点可以插入外源基因。其次,还增加了BEVS中可选择的启动子,除了多角体蛋白和p10启动子,AcMNPV中还有极早期启动子IE1和早中期启动子gp64。另外,异源性的启动子也能够应用于BEVS中,这些都加速了BEVS运用于科研及工业生产。
为了快速地推广BEVS,Summers和Smith在1987年一起编写了杆状病毒表达载体操作手册。随后,研究者利用BEVS成功地表达出了病毒样粒子(VLPs)。1987年Estes等人首次报道了用杆状病毒表达载体观察到猴轮状病毒VP6蛋白的自组装过程。1995年Powers等表达了流感A病毒亚单位疫苗抗原的重组血球凝集素,它的安全性及免疫效果都高于天然的疫苗。此后,BEVS广泛应用于疫苗、药物等的商业化生产。
1990年Kitts等人发现线性化的杆状病毒DNA能提高得到重组载体的效率(~ 25-30%)。1993年Kitts和Posses分别在野生型杆状病毒多角体蛋白基因的相邻基因ORF603上游和ORF1629下游插入了一个不常见的限制性酶切点位Bsu36I。用限制性内切酶Bsu36I切割后的AcMNPV DNA只有与外源基因重组后,才能够感染细胞。改造后的杆状病毒表达载体与带有外源基因的载体重组率达到了90%,这大大提高了重组病毒的筛选效率。随后,Luckow等人优化了这个系统,他们对AcMNPV DNA进行了改造,在多角体基因位点插入了大肠杆菌的mini-F复制子、卡那霉素抗性基因和细菌转座子att-Tn7。新的杆状病毒穿梭载体(AcMNPV bacmid)既能向像质粒一样在大肠杆菌中进行复制,也能感染鳞翅目的昆虫细胞。重组的杆状病毒DNA先从大肠杆菌中纯化出来,然后转染到昆虫细胞产生重组杆状病毒,这就是Bac-to-Bac系统。直到2003年,Ian Jones敲除了ORF1629的部分序列,使杆状病毒重组效率达到100%。
3 什么是Bacmid
1981年L. K. Miller根据AcMNPV分子生物学性质及现代分子生物学技术,从理论上阐述了杆状病毒作为载体表达外源基因的可行性。1983年G. E. Smith等成功地利用AcMNPV作为载体在草地夜蛾(Spodoptera frugiperda)细胞中表达了人β-干扰素基因,完成了从理论到实践的飞跃。1990年P. A. Kitts把一个Bsu36I位点引入到多角体基因附近。用Bsu36I线性化AcMNPV后,重组效率提高15-150倍,30%的空斑是阳性克隆。1993年P. A. Kitts把两个Bsu36I位点一起引入,结果使重组效率达到90%,但还是需要空斑筛选(多角体,蓝白斑)。
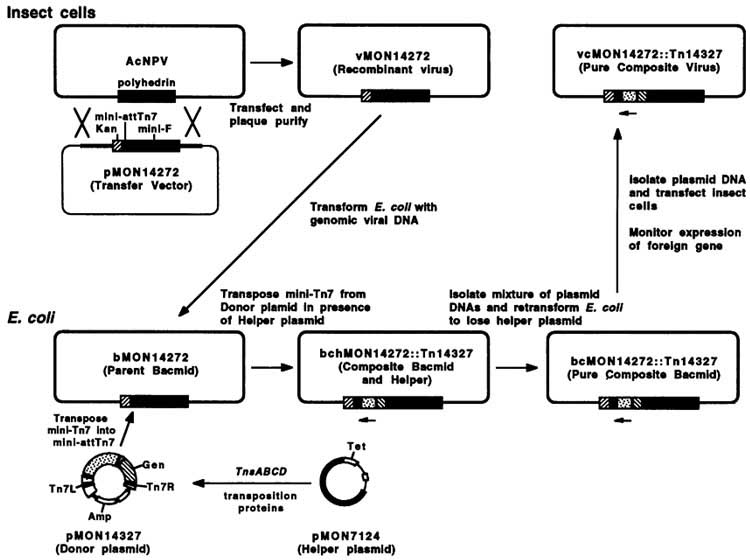
1993年V. A. Luckow用miniF-Kan替换了多角体基因,构建了能在昆虫细胞和大肠杆菌之间穿梭的杆状病毒重组DNA,命名为Bacmid。该名称取自Baculovirus和plasmid,中文译名为“杆粒”。
参考文献:
Miller LK. A virus vector for genetic engineering in invertebrates, p. 203-224. In N. J. Panopoulos (ed.), Genetic engineering in the plant sciences. Praeger, New York. 1981.
Smith GE, Summers MD, Fraser MJ. Production of human beta interferon in insect cells infected with a baculovirus expression vector. Mol Cell Biol. 1983 Dec;3(12):2156-65.
Kitts PA, Ayres MD, Possee RD. Linearization of baculovirus DNA enhances the recovery of recombinant virus expression vectors. Nucleic Acids Res. 1990 Oct 11;18(19):5667-72.
Kitts PA, Possee RD. A method for producing recombinant baculovirus expression vectors at high frequency. Biotechniques. 1993 May;14(5):810-7.
Luckow VA, Lee SC, Barry GF, Olins PO. Efficient generation of infectious recombinant baculoviruses by site-specific transposon-mediated insertion of foreign genes into a baculovirus genome propagated in Escherichia coli. J Virol. 1993 Aug;67(8):4566-79.
4 qBac®简介
qBac® Bacmid最初来源于英国牛津,2000年在雷丁改造成了免空斑筛选的Bacmid(Nucleic Acids Res. 2003, 31:E6-6;完全授权)。2009年由我们引进到国内,继续对其进行高产化改造,这些改造包括删除一些影响外源基因产量的非必需基因、插入抗凋亡小RNA片段,以及加入荧光蛋白使病毒感染可视化。我们的Bacmid载体系统化命名为qBac,其后用罗马数字标识代次。
qBac® Bacmid采用同源重组方式获得重组病毒,过程简便,优于目前广泛使用的Bac-to-bac系统。qBac® Bacmid获得带有外源基因的重组病毒的程序如下图所示:
关键词:昆虫细胞表达系统,杆状病毒表达载体系统,蛋白质表达,真核表达系统
 陕公网安备61909002000114号
陕公网安备61909002000114号

